Ферменти
визначення
Ферменти - це хімічні речовини, які можна знайти по всьому організму. Вони задають хімічні реакції в русі в організмі.
історія
Слово фермент був від Вільгельм Фрідріх Кюне 1878 року і походить від грецького слова ензимон, що означає дріжджі або закваску. Потім це знайшло свій шлях у міжнародній науці. The міжнародний союз чистої прикладної хімії (IUPAC) та міжнародний союз біохімії (IUBMB) розробили номенклатуру ферментів, яка визначає представників цієї великої групи речовин як загальну групу. Найменування, яке класифікує ферменти за їх завданнями, має важливе значення для визначення завдань окремих ферментів.
Ілюстрація ферментів
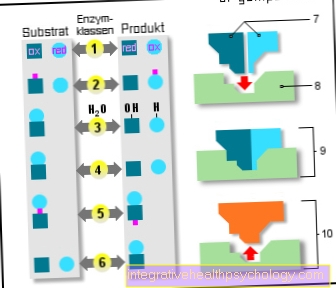
Ферменти
6 ферментних класів:
- Оксидоредуктази
(Окислення / відновлення) - Трансферази
(Спосіб передавання) - Гідролази
(Вживання води) - Лізи
(Розщеплення) - Ізомерази
(та ж молекулярна формула) - Лігази
(Реакції додавання) - Субстрати
- Активний центр
- Фермент / субстрат
складний - Фермент / продукт
складний
Огляд усіхЗображення Dr-Gumpert можна знайти за адресою: медичні ілюстрації
Іменування
The Іменування фермент включений три основні принципи заснований.Назви ферментів, які закінчуються на-описують кілька ферментів у системі. Сама назва ферменту описує реакцію, яку фермент запускає в рух (каталізується). Назва ферменту також є класифікацією ферменту. Крім того, кодова система, яка Система числення ЄС, в якій ферменти виробляються під числовим кодом чотири числа можна знайти. Перше число позначає клас ферментів. Списки всіх виявлених ферментів гарантують, що вказаний код ферменту можна швидше знайти. Хоча коди ґрунтуються на властивостях реакції, яку каталізує фермент, на практиці числові коди виявляються невиправданими. Систематичні назви на основі вищезазначених правил використовуються частіше. Проблеми з номенклатурою виникають, наприклад, з ферментами, які каталізують кілька реакцій. Тому іноді існує кілька назв для них. Деякі ферменти мають тривіальні назви, які не вказують на те, що згадана речовина є ферментом. Оскільки назви традиційно широко використовувались, деякі з них збереглися.
Класифікація за функцією ферменту
Відповідно до IUPAC та IUBMB, ферменти поділяються на шість ферментних класів відповідно до реакції, яку вони ініціюють:
- Оксидоредуктази
Оксидоредуктази встановлюють окислювально-відновні реакції в русі. У цій хімічній реакції електрони переходять від одного партнера реакції до іншого. Відбувається вивільнення електронів (окислення) однієї речовини та поглинання електронів (відновлення) іншою речовиною.
Формула каталізованої реакції - A ?? + B? A? + B?.
Речовина А виділяє електрон (?) І окислюється, а речовина В поглинає цей електрон і знижується. Ось чому окислювально-відновлювальні реакції називають також реакціями відновлення-окислення.
Багато метаболічних реакцій є окислювально-відновними реакціями. Оксигенази переносять один або кілька атомів кисню до їх субстрату. - Трансферази
Трансферази переносять функціональну групу з одного субстрату в інший. Функціональні групи - це атомні групи в органічних сполуках, які значною мірою визначають властивості речовини та реакційну поведінку. Хімічні сполуки, які мають однакові функціональні групи, групуються в класи речовин за своїми подібними властивостями. Функціональні групи поділять залежно від того, є вони гетероатомами чи ні. Гетероатоми - це всі атоми всередині органічних сполук, які не є ні вуглецем, ні воднем.
Напр .: -ОН -> гідроксильна група (спирти) - Гідролази
Гідролази розщеплюють зв’язки в оборотних реакціях, використовуючи воду. Ефіри, складні ефіри, пептиди, глікозиди, кислотні ангідриди або C-C зв’язки. Реакція рівноваги: A-B + H2O? A-H + B-OH.
Фермент, що належить до групи гідролаз, наприклад Альфа-галактозидаза. - Лізи
Лізази, які ще називають синтазами, каталізують відщеплення складних продуктів з простих субстратів, не розщеплюючи АТФ. Схема реакції - A-B → A + B.
АТФ - аденозинтрифосфат і нуклеотид, що складається з трифосфату нуклеозиду аденозину (і як такий енергетично багатий будівельний блок РНК нуклеїнової кислоти). Однак АТФ - це головним чином універсальна форма негайно доступної енергії у кожній клітині і водночас важливий регулятор процесів енергопостачання. При необхідності АТФ ресинтезується з інших запасів енергії (креатинфосфат, глікоген, жирні кислоти). Молекула АТФ складається з залишку аденіну, рибози цукру та трьох фосфатів (? До?) В ефірі (?) Або ангідридних зв'язків (? І?). - Ізомерази
Ізомерази прискорюють хімічну конверсію ізомерів. Ізомерія - це виникнення двох або більше хімічних сполук з абсолютно однаковими атомами (однакова емпірична формула) і молекулярних мас, які, однак, відрізняються між собою зв’язком або просторовим розташуванням атомів. Відповідні сполуки називають ізомерами.
Ці ізомери відрізняються за своїми хімічними та / і фізичними, а часто і за біохімічними властивостями. Ізомерія виникає насамперед з органічними сполуками, але також з (неорганічними) координуючими сполуками. Ізомерія поділяється на різні області. - Лігази
Лігази каталізують утворення речовин, які є хімічно складнішими за використовувані субстрати, але, на відміну від ліаз, є лише ферментативно активними шляхом розщеплення АТФ. Тому для утворення цих речовин необхідна енергія, яка отримується шляхом розщеплення АТФ.
Деякі ферменти здатні каталізувати кілька, іноді дуже різні реакції. Якщо це так, їх призначають до кількох ферментних класів.
Можливо, вам також будуть цікаві такі статті:
- Альфа-глюкозидаза
- Ліпаза
- Трипсин
Класифікація за структурою ферменту
Майже всі ферменти є білками і їх можна класифікувати за довжиною білкової ланцюга:
- Мономери
Ферменти, які складаються лише з одного білкового ланцюга - Олігомери
Ферменти, що складаються з кількох білкових ланцюгів (мономерів) - Мультиферментні ланцюги
Кілька агрегованих ферментів, які взаємодіють і регулюють один одного. Ці ланцюги ферментів каталізують послідовні кроки в метаболізмі клітини.
Крім того, існують окремі білкові ланцюги, які містять кілька ензимних активностей; їх називають багатофункціональними ферментами.
Класифікація за коефіцієнтами
Інша класифікація - класифікація відповідно до кофакторів. Кофактори, коферменти та ко-субстрати - це назви різних класифікацій речовин, що впливають на біохімічні реакції завдяки їх взаємодії з ферментами.
Розглядаються органічні молекули та іони (переважно іони металів).
Чисті білкові ферменти складаються виключно з білків, а активний центр утворюється лише з амінокислотних залишків і пептидної основи. Амінокислоти - це клас органічних сполук, що мають принаймні одну карбоксигрупу (-COOH) та одну аміногрупу (-NH2).
Холоензими складаються з білкового компонента, апоензиму та кофактора, молекули низької молекулярної маси (не білка). Обидва разом важливі для функції ферменту.
Коферменти
Органічні молекули як кофактори називають коферментами. Якщо вони ковалентно пов'язані з апоензимом, їх називають протезними групами або ко-субстратами. Протезова група - це термін, що використовується для опису небілкових компонентів, міцно (як правило, ковалентно) пов'язаних з білком з каталітичним ефектом.
Косубстрати - це назви різних класифікацій речовин, які впливають на біохімічні реакції завдяки їх взаємодії з ферментами. Як біокаталізатори, молекули прискорюють реакції в організмах, ферменти прискорюють біохімічні реакції. Вони зменшують енергію активації, яку треба подолати, щоб речовина могло перетворитися.